Quand le LBPA résiste au VIH

Un laboratoire, deux équipes en synergie contre le VIH
Au cœur de l'Institut d'Alembert, deux équipes du LBPA travaillent de concert pour comprendre les mécanismes de fonctionnement du VIH-1 (Virus de l'Immunodéficience Humaine) responsable du sida.
Olivier Mauffret, directeur de recherche CNRS à l’ENS Paris-Saclay, dirige l’équipe « Structures et interactions des acides nucléiques », composée d’une dizaine de chercheurs, doctorants et techniciens. Elle est spécialisée dans l’étude du processus de transcription inverse avec des expertises sur les protéines transcriptase inverse et la nucléocapside. Cette dernière protéine est essentielle pour faciliter les transferts de brin qui se produisent lors de la transcription inverse. Différentes techniques de biophysique et de biologie moléculaire sont utilisées pour comprendre les mécanismes de développement et réplication du virus.
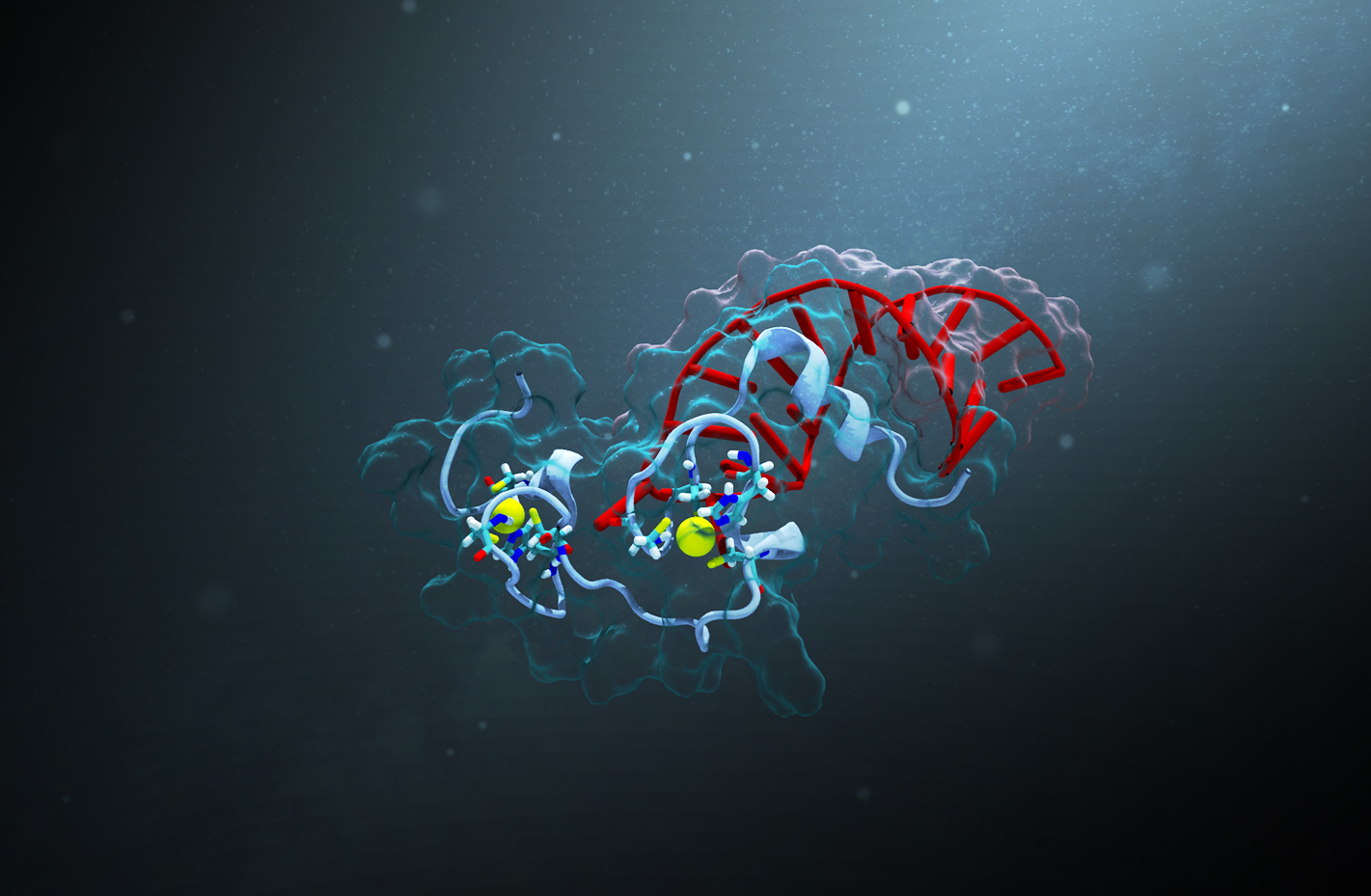
Une vue du complexe entre la protéine de nucléocapside et la tige boucle ARN SL3" - vue réalisée par R. Retureau (LBPA)
Olivier Mauffret utilise la spectroscopie RMN pour observer et récolter des données moléculaires tri-dimensionnelles sur les acides nucléiques qui jouent un rôle déterminant dans les processus de transfert de brin. Le but de ces recherches est de comprendre les bases moléculaires de ces événements essentiels dans la recombinaison génétique rétrovirale.
Philippe Fossé, directeur de recherche CNRS au sein de cette même équipe, détermine les structures secondaires des ARN impliquées dans les processus de transcription inverse avec des outils de biologie moléculaire et des agents chimiques. Il travaille « in vitro », reconstituant les étapes du cycle réplicatif du VIH dans un tube à essai avant de tester ses hypothèses « in cellulo », directement dans une cellule infectée. Il travaille depuis peu en étroite relation avec l’équipe « Biophotonique des interactions moléculaires » du LBPA, dirigée par Eric Deprez, et en particulier avec le chercheur et virologue Olivier Delelis. Cette collaboration permet à Philippe Fossé de vérifier l’impact de la structuration des ARNs sur les processus de transfert de brin et de réplication du virus. Ses hypothèses seront testées à partir de mutagénèses dirigées et de PCR quantitative – au sein de l’équipe « Biophotonique » – pour quantifier l'ADN de manière précise.
Un nouveau mécanisme de résistance du VIH-1 à l’anti-intégrase
L’équipe « Biophotonique des interactions moléculaires » du LBPA est spécialisée dans les processus d’intégration et dans l’analyse de la protéine intégrase. Olivier Delelis, Directeur de recherche CNRS à l’ENS Paris-Saclay y étudie différents types de virus, dont le VIH-1 depuis plusieurs années. L’activité de l’équipe consiste à tester les composés pharmacologiques qui inhibent la réplication du VIH mais surtout à comprendre comment celui-ci se réplique à partir d’expériences sur différents types de cellules.
Alors que l’avènement des traitements antirétroviraux depuis vingt ans a permis de mettre le VIH « sous contrôle » pour une majorité des patients porteurs du virus, Olivier a découvert, il y a deux ans, avec la contribution de son équipe et des professeurs Anne-Geneviève Marcellin et Vincent Calvez, cliniciens à l’Hôpital Pitié Salpêtrière, un nouveau mécanisme de résistance à l’anti-intégrase chez 15% des patients recevant le traitement anti-VIH du Dolutégravir. Autrement dit, ces patients échappent, pour des raisons qui étaient jusqu’ici inconnues, au traitement alors que la molécule est connue pour être très efficace.
Le début de cette collaboration avec les cliniciens de la Salpêtrière remonte à plus de 10 ans et les premières mutations de résistance aux anti-intégrases ont donné lieu à plusieurs publications scientifiques explique Olivier Delelis qui a présenté les résultats de ces travaux à la CROI - Conference on Retroviruses and Opportunistic infections - qui rassemble chaque année 3 000 personnes venant du monde entier. « On a montré qu’il y avait une mutation sélectionnée à un endroit du génome viral qui apportait de la résistance à l’anti-intégrase. Normalement quand il y a une résistance c’est plutôt au niveau de la protéine. Là c’est sur une autre partie du génome. »
Olivier Delelis reste humble et confiant « Nous souhaitons aller encore plus loin dans nos vérifications. Si le modèle que l’on a proposé s’avère vrai, il sera possible d’expliquer une grande partie des échecs thérapeutiques chez les patients. D’ailleurs d’autres groupes de chercheurs (en Angleterre, …) ont mis en évidence les mêmes mutations que nous avons observées. »
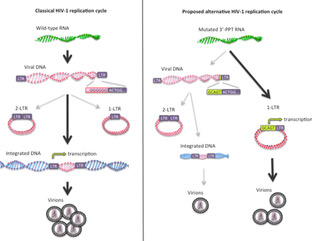
Photo en haut de l'article : les deux équipes du LBPA "Biophotonique des interactions moléculaires" et "Structures et interactions des acides nucléiques" travaillant sur le VIH-1 devant le laboratoire sécurisé dédié aux recherches sur les virus et bactéries pathogènes
Crédit photo : communication ENS Paris-Saclay - Alfonso Rodriguez